Chapitres
Le roentgenium est un élément chimique qui porte le numéro 111 dans la classification périodique des éléments. 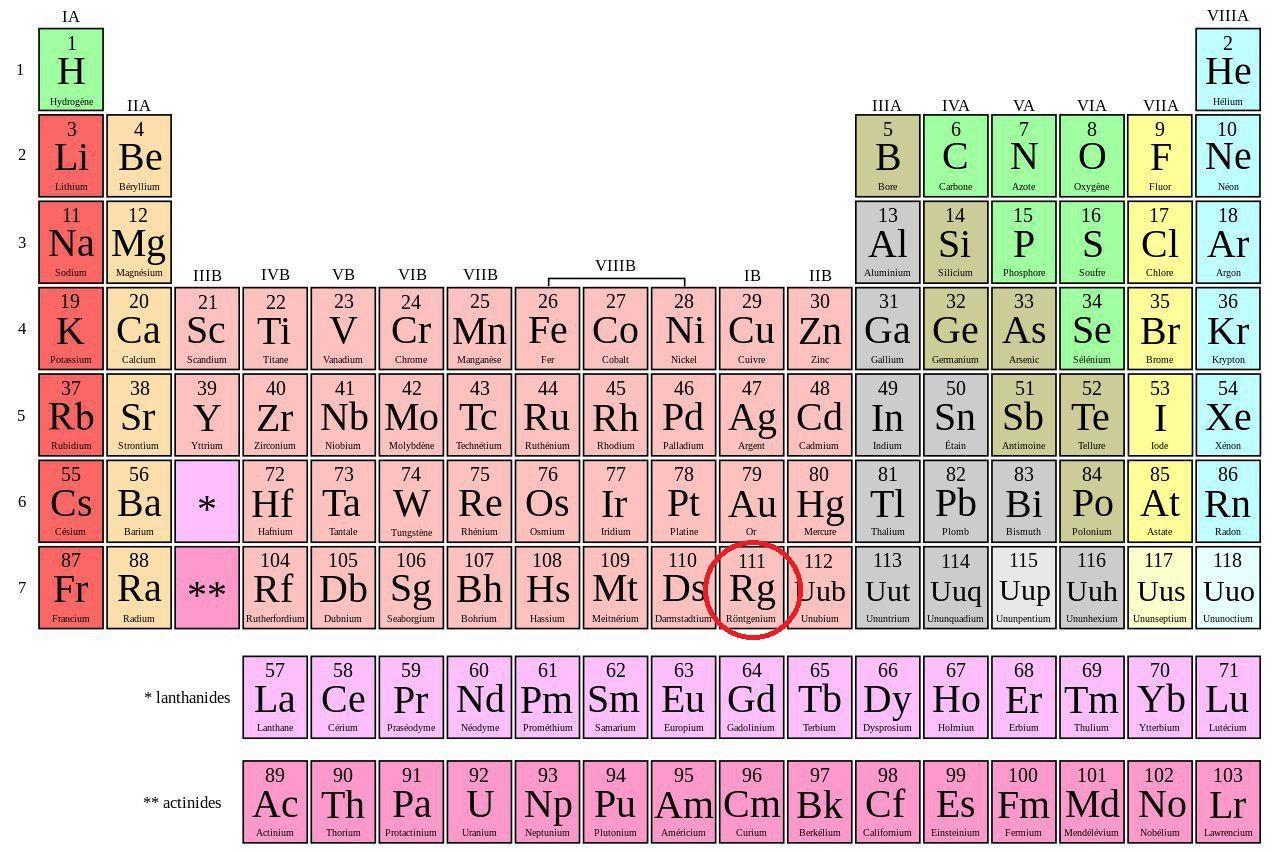
| Informations générales | |
|---|---|
| Symbole | Rg |
| Numéro atomique | 111 |
| Famille | Métal de transition |
| Groupe | 11 |
| Période | 7 |
| Bloc | d |
| Masse volumique | 28,7 g.cm-3 |
| Propriétés atomiques | |
| Masse atomique | 282 |
| Configuration électronique | [Rn] 7s2 5f14 6d9 |
| Électrons par niveau d'énergie | 2 | 8 | 18 | 32 | 32 | 17 | 2 |
| Propriétés physiques | |
| État ordinaire | Solide |
Définitions
- Numéro atomique : Le numéro atomique d'un atome représente le nombre de protons de ce dernier
- Famille : L'UICPA (Union internationale de chimie pure et appliquée) a regroupé en 10 familles les éléments chimiques qui présentent des propriétés physiques et chimiques semblables
- Groupe : Chaque groupe correspond aux éléments chimiques présents dans une même colonne du tableau périodique des éléments
- Période : Chaque période correspond aux éléments chimiques présents dans une même ligne du tableau périodique des éléments. Ils partagent également le même nombre de couches électroniques. On en compte 7 au maximum
- Bloc : Les éléments périodiques sont classés par bloc selon leurs propriétés et selon les couches électroniques jusqu’auxquelles elles sont remplies
- Dureté : La dureté d'un matériau représente la résistance qu'il oppose à la pénétration. On peut la mesurer selon plusieurs méthodes : la méthode par pénétration, la méthode par rayage ou encore la méthode par rebondissement
- Point de fusion : Le point de fusion correspond à un moment de pression et de température à partir duquel l'élément chimique fond, passant ainsi de l'état solide à l'état liquide
- Point d'ébullition : Le point d'ébullition correspond à un moment de pression et de température à partir duquel l'élément chimique bout, passant ainsi de l'état liquide à l'état gazeux
Rappel : La classification périodique des éléments, aussi appelée tableau de Mendeleïev, du nom de son créateur. C'est un chimiste russe qui en 1869 créa un tableau dont le but était de regrouper tous les éléments chimiques connus par points communs (groupes et familles par exemple). Il a souvent été ajusté et mis à jour depuis cette époque. Sa dernière révision date de 2016 par l'UICPA (Union internationale de chimie pure et appliquée), une ONG suisse qui a pour but l'évolution de la physique-chimie. Le tableau périodique compte à ce jour 118 éléments. L’UICPA, l’Union Internationale de Chimie Pure et Appliquée est une organisation non gouvernementale ayant son siège à Zurich, en Suisse. Créée en 1919, elle s’intéresse au progrès de la chimie, de la chimie physique et de la biochimie. Ses membres sont les différentes sociétés nationales de chimie et elle est membre du Conseil International pour la Science. L’UICPA est une autorité reconnue dans le développement des règles à adopter pour la nomenclature, les symboles et autres terminologie des éléments chimiques et leurs dérivé via son Comité Interdivisionnel de la Nomenclature et des Symboles. Ce comité fixe la nomenclature de l’UICPA.

Un peu d’histoire autour du roentgenium
Son étymologie
Le roentgenium tient son nom du physicien allemand Wilhelm Conrad Röntgen. 
Wilhelm Conrad Röntgen
Wilhelm Conrad Röntgen est un physicien originaire d’Allemagne et ayant vécu entre 1845 et 1923. Il est notamment connu pour avoir découvert les rayons X. Cette découverte lui valut également de recevoir le premier prix Nobel de l’histoire en 1901, celui de physique.
La première découverte du roentgenium
Le roentgenium fut synthétisé pour la première fois en 1994 par deux chercheurs allemands du GSI, le centre de recherches sur les ions lourds de Darmstadt, Peter Armbruster et Gottfried Münzenberg. L'isotope qu'ils réussirent à obtenir était du roentgenium 272. Ils l'obtinrent en fusionnant deux noyaux atomiques : un noyau de bismuth 209 et un noyau de nickel 64.
Peter Armbruster
Peter Armbruster est un physicien allemand né en 1931. Il est originaire de Dachau, en Bavière. Après des études de physique, il est diplômé d'un doctorat en 1961. Il a commencé ses recherches dans les domaines de la fission, des ions lourds er de leurs interactions avec des produits de fission au Centre de recherche de Jülich situé lui aussi en Allemagne. Il par ensuite au Centre de recherche sur les ions lourds à Darmstadt où il va découvrir avec l'aide de son partenaire Gottfried Münzenber de nombreux éléments comme :
- Le darmstadtium,
- Le bohrium,
- Le meitnérium,
- Le roentgenium,
- Le copernicium,
- L'hassium.
Il continue ensuite sa carrière en France, à Grenoble, à l'Institut européen de Laue-Langevin jusqu'en 1992. Depuis 1996, il fait partie d'un projet de recherche concernant l'incinération des déchets nucléaires par réactions de spallation et de fission. La spallation nucléaire est une réaction nucléaire lors de laquelle on fait entrer en collision un noyau avec une autre particule comme un neutron ou un proton ou avec une onde électromagnétique très puissante. Cette collision crée alors une décomposition du noyau laissant échapper des particules comme des neutrons, des protons ou des noyaux plus légers comme des noyaux d’hélium ou de lithium Il a été récompensé de nombreuses fois par les distinctions suivantes :
- Ordre du mérite de Hesse,
- Prix Max-Born,
- Médaille Stern-Gerlach,
- Prix Lise Meitner.
Centre de recherche sur les ions lourds
Le Centre de recherche sur les ions lourds, Gesellschaft für Schwerionenforschung mbH en Allemand, souvent abrégé en GSI, est un centre allemand, situé dans la ville de Darmstadt qui effectue des recherches dans plusieurs domaines :
- La physique des particules,
- La physique nucléaire,
- La chimie nucléaire,
- La physique de la matière,
- La biophysique.
Il a été créé dans le but de réunir plusieurs universités. Celles de Darmstadt, Francfort, Mayence, Hidelberg et Giessen afin de mettre au jour un centre de unique de recherche dans le domaine de la physique nucléaire. Aujourd'hui, ses principales actions sont la synthétisation d'éléments dits superlourds comme le darmstadtium par exemple. Ils se sont aussi spécialisés dans la proton-thérapie, une méthode médicale de radiothérapie pour tuer les cellules cancéreuses du corps humain.
La présence à l’état naturel de l'élément 111

Propriétés physiques et chimiques
Le roentgenium est un élément faisant partie des transactinides.
On appelle transactinide tout élément chimique dont le numéro atomique est supérieur à celui du lawrencium (103), le dernier des actinides. Ce sont également les éléments appelés superlourds. Qui sont, par définition, également des transuraniens, ayant un numéro atomique supérieur à celui de l’uranium (92). Il est important de savoir que, parmi les transuraniens, les transactinides présentent certaines particularités
On ne connaît pas de caractéristiques à cet élément qui n'a pas été suffisamment produit, ce qui explique qu'il reste pas mal de zones d'ombre à son sujet.
Les isotopes du roentgenium
Des isotopes sont des atomes qui possèdent le même nombre de protons mais un nombre différent de neutrons
Le roentgenium étant un élément synthétique, il n'existe aucun isotope stable de ce dernier. On lui connait 7 radioisotopes avec des nombres de masse allant de 272 à 282.
Le nombre de masse d’un atome est le nombre de nucléons qu’il contient. Il s’agit donc de la somme du nombre de protons et du nombre de protons qui constituent le noyau de l’atome
L'isotope qui a la plus longue durée de vie est le roentgenium 282 avec une durée de demie-vie de 2,1 minutes. Celui qui a la plus petite durée de demie-vie est le roentgenium 272 qui a une durée de demie-vie de 2 ms.
Utilisations
Aucune utilisation commerciale ou industrielle n'est attribuée au roentgenium. Cet élément n'est pas assez produit pour qu'on en sache assez sur ces caractéristiques et ses utilisations potentielles.
Dangers potentiels du roentgenium

On dit d’un objet qu’il est écotoxique lorsqu’il est toxique pour l’environnement, c’est-à-dire polluant
De plus, comme sa durée de demie-vie dépasse à peine une dizaine de minutes au maximum, même s'il s'en retrouvait dans l'environnement cela n'aurait pas d'impact important sur ce dernier.























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !