Chapitres

La dualité onde-particule
La lumière est une onde électromagnétique. Cependant, certaines de ses caractéristiques démontrent qu'elle se comporte également comme un ensemble de particules : c'est ce que l'on appelle la dualité onde-particule (généralisée en "dualité onde-corpuscule" lorsqu'on considère tous les objets de l'univers microscopique).
Historique
Au XVIIème siècle, le physicien néerlandais Huygens donne la théorie ondulatoire de la lumière : les ondes lumineuses peuvent interférer de manière à former un front d'onde se propageant en ligne droite. Cette théorie sera confirmée par les expériences de Young et Fresnel sur la diffraction au début du XIXème siècle.
En 1672, Newton propose une théorie opposée à celle de Huygens sur la lumière, qui serait constituée de "petites particules".
Les équations de Maxwell, à la fin du XIXe siècle, expliquent la lumière en tant que propagation d'ondes électromagnétiques.
Enfin, en 1905, Einstein réconcilie la théorie de Huygens avec celle de Newton. Il postule l'existence de « particules » transportant des quanta d'énergie lumineuse. La fréquence v de cette lumière est liée à l'énergie E de ces particules par la constante de Planck.
Quelques années plus tard, Lewis les qualifie de « photons ».
Caractéristiques de l’onde lumineuse
Une onde électromagnétique comme la lumière se propage sans milieu matériel. La lumière est une onde sinusoïdale et vectorielle car l’énergie lumineuse est portée par une onde électromagnétique. Elle est formée par un champ électrique E et un champ magnétique B perpendiculaire entre eux, en phase (de même longueur d’onde), et perpendiculaires à la direction de propagation de l’onde : l’onde lumineuse est donc transversale.
Qu'est-ce qu'un photon ?
L'énergie de la lumière est divisée en paquets bien définis que l'on appelle quanta (quantum au singulier). Les quanta sont associés à des particules appelées photons.
Les photons sont donc les particules élémentaires qui composent la lumière. Le photon n’est cependant pas uniquement associé à la lumière, mais à toutes les ondes électromagnétiques.
La physique quantique classe le photon dans la catégorie des bosons : c’est donc une particule de spin (on parle aussi de moment cinétique, qui pourrait être assimilé à une rotation de la particule sur elle-même) entier.
Les caractéristiques des photons
Un photon est une particule qui possède une masse nulle, qui n'a pas de charge électrique (mais possède deux état de polarisation) qui se déplacent en permanence à la vitesse de la lumière. Lors du passage dans un milieu matériel, l’énergie du photon est invariante car la fréquence est invariante.
L'énergie des photons
L'énergie d'un photon dépend uniquement de la fréquence de la lumière. Cette énergie peut être calculée grâce à la relation suivante :
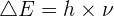
Dans cette formule :
- ΔE est le quantum d'énergie associé au photon et exprimé en joule (J)
- h est la constante de Planck : h = 6,63 x 10-34s
- ν est la fréquence de la lumière en hertz (Hz)
Par ailleurs il est aussi possible d'exprimer l'énergie d'un photon en fonction de sa longueur d'onde. On sait que :
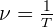
De même :

On peut donc en déduire une nouvelle expression de la fréquence :
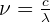
Ainsi, l'énergie peut être exprimée de la façon suivante :

Avec toutes les données précédentes, il est également possible de simplifier cette formule, avec l'énergie en électronvolts (eV) plutôt qu'en joules (J), et la longueur d'onde en nanomètres (nm).

Un électron-Volt correspond à l’énergie cinétique acquise par un électron accéléré depuis le repos par une différence de potentiel de 1V. Il est possible d’effectuer la conversion suivante : 1 eV = 1,602 x 10-19
Interaction des photons avec la matière
Interaction avec les électrons
Les photons ont initialement été décrits par Einstein d’après leur interaction avec les électrons. En effet, c’est en tentant d’expliquer l’effet photoélectrique qu’Einstein émit l’hypothèse des « quanta d’énergie » constituant la lumière.
L’effet photoélectrique est lié à l’intégration entre un photon et un électron. Lorsqu’un photon est projeté au sein du nuage électronique d’un atome, notamment au sein des couches électroniques les plus profondes, l’énergie E de ce photon peut être totalement transférée à l’électron, qui est ainsi éjecté hors de l’atome.
- L’atome est ionisé et le photon disparaît : on parle d’absorption totale.
- Il est également possible que le photon ne soit pas totalement absorbé : on parle alors de diffusion.
- Si un photon, le plus souvent de faible énergie, passe à proximité du nuage électronique d’un atome, il ne sera que dévié sans modification d’énergie : on parle de diffusion simple (cohérente et élastique).
Ce phénomène n’entraîne pas d’ionisation. Dans le cas d’une diffusion Compton (considérée comme une diffusion incohérente ou inélastique), qui concerne principalement les électrons des couches externes dans les atomes possédant un numéro atomique Z élevé, le photon incident cède (en étant dévié mais pas absorbé) une partie de son énergie à l’électron, qui sera alors éjecté formant un électron Compton. L’atome est ionisé.

Lors de l’éjection de l’atome, l’énergie du photon incident se divise entre le photon diffusé et l’électron sous forme d’énergie cinétique. Si le photon est absorbé, toute son énergie est transférée à l’électron.
Interaction avec les noyaux
Si l'énergie du photon incident à proximité d'un noyau est supérieure à 1,022 MeV, ce photon peut se matérialiser en une paire électron-positon. L'énergie du photon va se répartir également entre ces deux particules. Une fois l’énergie cinétique épuisée, le position va s'annihiler : en rencontrant un électron, le position va émettre deux photons de 511 keV, partant à 180° l'un de l'autre.
Un photon de haute énergie peut également être absorbé par le noyau, qui devient instable et se désintègre en émettant un neutron : c'est l'effet photonucléaire.
AZX + 00Ɣ → A-1ZX + 10n
Cette réaction permet la formation d’un isotope du noyau X, qui sera généralement radioactif.
Utilisation des photons dans la vie courante
Les photons servent essentiellement à produire de la lumière. Ces particules sont donc présentes dans les rayons de nos ampoules, celles du Soleil ou des lasers.
Mais elles ont également une application plus technique.
En effet, les photons trouvent une application dans le milieu médical à travers l’imagerie. Par exemple, la tomodensimétrie (TDM) est basé sur le principe du contraste radiologique, ce qui permet de coder une image radiologique en niveau de gris selon la densité des milieux traversés.























Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Bonjour s’il vous plais j’ai besoin de l’interprétation physique de l’interaction photon-atome
Bonjour, je dois décrire les étapes qui permettent aux photons émis par la lumière solaire arrivant sur la cellule de délivrer un courant électrique, mais je ne comprends pas. Pourriez vous m’aider svp ?
Merci
Bonjour j’ai besoin des exercices sur l’énergie d’un photon et calcul de la longueur d’onde seuil
Bonjour, nous serions ravis de vous aider ! Rendez-vous sur la plateforme de Superprof, sélectionnez la rubrique « Découvrir nos Superprofs » en indiquant la matière souhaitée. Vous trouverez de nombreux professeurs près de chez vous. Bonne journée ! 🙂
Bonjour,
Merci pour ce cours, il y a juste une petite erreur d’inattention sur l’unité de h qui est en J.s . Rien de bien dérangeant mais j’avoue que ça m’a mis le doute ^^ , pourriez- vous le corriger svp ?
Merci
Merci pour ton commentaire Mathilde!
Merci professeur
Bonjour, j’aimerais savoir un un unique photon, vu comme une onde, peut être émis dans toutes les directions de l’espace, ou s’il est émis dans un cône, ou dans une direction précise.