Chapitres

Définition de l'absorbance
L’absorbance est une grandeur physique qui traduit la capacité d’un milieu à absorber un rayonnement.
Ainsi une solution colorée absorbe une partie de la lumière, on parle d’absorbance de la solution. L’absorbance dépend essentiellement de deux paramètres :
- la concentration de la solution
- et la longueur d’onde de la lumière qui traverse la solution.
L’absorbance est donc une grandeur liée à l’intensité de la lumière de longueur d’onde λ absorbée en solution. Rappel : la concentration d’une solution est définie par le rapport n = C.V soit C= n/V avec C la concentration en mol/l et V le volume en litres et n le nombre de moles exprimé en mol.
Notation et unité
L’absorbance se note A, c’est une grandeur qui ne possède pas d’unité. Le saviez-vous ? L’absorbance est aussi appelée densité optique. On utilise cette grandeur en chimie mais aussi en biochimie et dans le domaine de la photographie. On peut aussi également rencontrer les termes extinction ou opacité. La densité optique, en photographie est équivalente à l’absorbance en spectrométrie. Elle est plus souvent définie à partir de la transmittance. La densité optique ou absorbance désigne alors le logarithme décimal de l'opacité, c'est à dire l'inverse de la transparence. La densité optique est utilisée notamment pour caractériser les filtres colorés, les filtres correcteurs de température de couleur ou pour mesurer la transparence du négatif photographique.
Relation entre absorbance et intensité
Elle est définie comme le logarithme décimal du rapport de l’intensité lumineuse (I0) du rayonnement incident divisé par l’intensité (I) du rayonnement émergent (d’où l’absence d’unité), ce qui peut se traduire par la relation suivante: A = Log ( Io/I) où I et Io sont exprimées dans la même unité
Conséquence de la relation entre absorbance et Intensité
D’après cette relation :
- L’absorbance est toujours supérieure à zéro car Io est toujours supérieure à I
- Lorsque le rayonnement n'est pas absorbé alors I = Io et A = 0 dans ce cas le milieu traversé est transparent
- L’absorbance n’est pas définie pour un milieu qui absorbe la totalité du rayonnement car dans ce cas le I tend vers zéro, le rapport Io/I tend vers l’infini ainsi que l’absorbance A
Quels sont les facteurs dont dépend l'absorbance ?
L’absorbance dépend :
- De l’épaisseur du milieu traversé
- De la composition du milieu
- De la longueur d’onde incidente (un même milieu peut être transparent à certaines longueurs d’onde et totalement opaque à d’autres.)

Loi de Beer-Lambert
Historique de la loi de Beer-Lambert
La loi de Beer-Lambert est aussi appelée loi de Bougier, surtout en France, mais pourquoi ?
Contrairement à ce qu’on pourrait penser, la paternité de la loi de Beer-Lambert est partagée par non pas deux mais trois scientifiques. La loi a tout d’abord été édictée par le mathématiciens et physicien français, Pierre Bougier, au XVIIIème siècle, dans sa publication « Essai optique sur la gradation de lumière ».
Les travaux de Pierre Bougier sont ensuite repris par Jean-Henri Lambert, considéré comme le père de la photométrie, quelques années plus tard.
Au siècle suivant, le scientifique allemand August Beer reprend et perfectionne la loi, qui prend sa forme actuelle et le nom de celle-ci associe alors le nom de Beer et celui de Lambert.
Loi de Beer-Lambert
La loi de Beer-Lambert permet d’établir une relation entre l’atténuation de la lumière et des propriétés du milieu que la lumière traverse. Elle est donnée par la relation suivante :
A = ε. l. c
Avec A qui désigne l’absorbance (sans unité) l désigne la longueur du trajet optique (en mètres) et c désigne la concentration de la substance en solution en mol/l. Enfin ε est le coefficient d’extinction molaire exprimé en l/mol. Attention, pour que la loi de Beer-Lambert fonctionne, elle doit obéir à quelques conditions :
- La lumière utilisée doit être monochromatique
- La solution ne doit pas être trop concentrée en sels incolores
- La solution ne doit pas être trouble
- Il ne doit pas y avoir de précipité
Le saviez-vous ? La loi de Beer-Lambert peut être appliquée pour décrire l'atténuation du rayonnement solaire à travers l'atmosphère. Dans ce cas, une partie de cette lumière est diffusée alors qu'une autre est absorbée par les différents constituants. Cette application permet de mettre en relation l’impact de la pollution sur l’atmosphère.
La spectrophotométrie
La spectrophotométrie permet de mesurer l’absorbance (appelée aussi densité optique) d’une substance en solution. Pour mesurer cette absorbance, on utilise un spectrophotomètre.

Comment fonctionne un spectrophotomètre ?
Le spectrophotomètre comprend tout d’abord une source de lumière. Celle-ci va ensuite passer dans un monochromateur (réseau diffractant la lumière de la source) qui va sélectionner une longueur d’onde.
La lumière d'intensité I0 va ensuite traverser une cuve qui contient la solution a analyser.
La lumière transmise I est ensuite analysée. (en passant par une cellule photoélectrique et un amplificateur).
Spectrophotomètre et longueur d’onde
Si on mesure l’absorbance d’une solution a différentes longueurs d’onde, on s’aperçoit qu’il existe une longueur d’onde pour laquelle l’absorbance est maximale. La couleur de la solution correspond alors à la couleur complémentaire.
- Rappel : qu’est ce qu’une longueur d’onde ?
Les ondes électromagnétiques sont définies par une longueur d’onde. La longueur d’onde correspond à la périodicité spatiale d’oscillations ou distance parcourue entre deux oscillations. On note la longueur d’onde λ. Le spectre de lumière représente l’ensemble des longueurs d’onde dont elle est constituée. Chaque longueur d’onde correspond à une couleur. Le spectre des couleurs visibles s’étend du rouge au violet. De part et d’autre du spectre visible on trouve les infrarouges et les ultraviolets non visibles. Les longueurs d’onde du spectre visible se situent entre 400 et 700 nm. Chaque couleur correspond à une longueur d’onde, ainsi on trouve :
- Le rouge entre 620 et 700 nm
- L’organe entre 592 et 620 nm
- Le jaune entre 578 et 592 nm
- Le vert entre 500 et 578 nm
- Le bleu entre 446 et 500 nm
- Le violet entre 400 et 446 nm
Note : une solution colorée absorbe la lumière, l’absorbance est fonction de la concentration de la solution et de la lumière qui traverse la solution. Pour connaître la concentration d’une solution, on peut réaliser une courbe d’étalonnage. 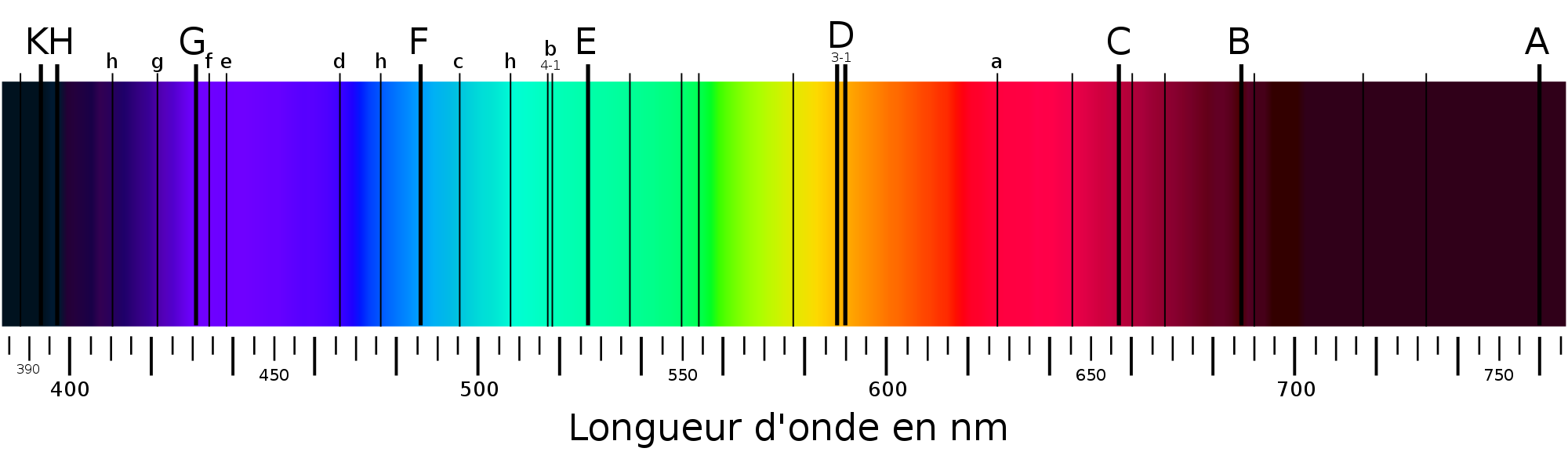
| Couleur absorbée | Couleur complémentaire |
|---|---|
| Rouge | Vert-bleu |
| Vert-bleu | Rouge |
| Bleu | Jaune |
| Violet | Jaune-vert |
Absorbance d’une solution aqueuse : mise en application
Elle dépend de la concentration de la solution (elle lui est proportionnelle). Elle peut être calculée grâce à la loi de Beer Lambert et mesurée à l’aide d’un spectroscope Une des applications de l’étude de l’absorbance et de la loi de Beer-Lambert est la possibilité de trouver la concentration d’une solution grâce à la technique de dosage par étalonnage.
Comment procède-t-on ?
On dispose d’une solution S de concentration connue et d’un échantillon de cette solution de concentration inconnue. Pour connaître la concentration d’une telle solution, on réalise tout d’abord une courbe d’étalonnage en utilisant des concentrations diluées de la solution mère S. Les dilutions effectuées, on utilise un spectrophotomètre calibré avec une longueur d’onde définie. Les résultats de l’absorbance permettent de réaliser un courbe A = f(T). Il s’agit d’une droite qui passe par l’origine et qui montre que l’absorbance est une fonction linéaire de la concentration. Il ne reste plus qu’à trouver sur la courbe établie le point qui corrèle l’absorbance de la solution inconnue. En projetant sur l’axe de la concentration, on trouve la valeur de la concentration de la substance inconnue. Note : si une solution comporte plusieurs espèces colorées (C1 et C2), l’absorbance est alors égale à la somme des absorbances dues à chaque espèces colorées






















Si vous désirez une aide personnalisée, contactez dès maintenant l’un de nos professeurs !
Bonsoir,
Je veux savoir si Lorsqu’on étudie la variation de l’absorbance d’une solution en fonction de la concentration du soluté, quels sont les autres acteurs qui ne doivent pas varier?
Bonjours une concentration de 0,50ppm d’une solution de l’or dont la catholique a une longueur d’onde de 4222.8 , quelle sera son absorbance
que se passe-t-il au point de vue moléculaire
J’aimerais savoir pourquoi le fait d’utiliser la longueur d’onde maximale vient diminuer l’incertitude lorsqu’on fait des calculs en colorimétrie?
bonjour ! comment savoir A en fonction de la longueur d’onde
Bonjour, si vous cherchez toujours réponse à votre question, je vous invite à consulter nos professeurs qui vous aideront avec plaisir 🙂
Svp, pourquoi on effectue une dilution àvant faire les mesures spectrométriques ?